化工基础知识-有机物基础
有机化合物简称有机物,是指碳氢化合物及其衍生物,有机化学是研究碳氢化合物及其衍生物的化学。
(1)熔点较低,多数有机化合物的熔点在300℃以下。
(2)容易燃烧,多数有机化合物燃烧后变成CO2和H2O。
(3)难溶于水,易溶于有机溶剂中。
(4)有机化合物不能电离,也不能导电,是非电解质。
(5)化学反应复杂,还伴有副反应发生,反应速度缓慢,且不易完成。
有机化合物除了主要元素以外,还含有少数几种其它元素,如H、O、S、P和卤素等。它们之间的结合,排列和相互影响,就在于碳的特殊性质。碳元素在形成化合物时,它既不易失去电子而形成正离子也不易获得电子而形成负离子,而是以共价键与其它原子相结合,即碳原子以四根键同其它非金属元素或金属元素结合形成分子。
例如:四氯化碳(四氯甲烷)
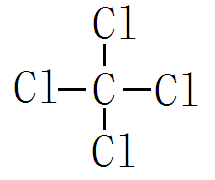
碳原子不仅能与其它原子形成共价键,碳原子与碳原子之间也能以共价键相结合,它们可以共用一个、两个或三个电子对,形成单键、双键或三键。
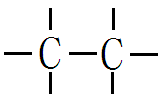
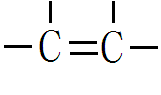
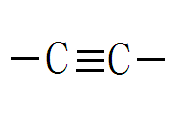
碳原子之间还可以相互结合成链状、环状、网状的有机化合物的基本骨架。
有机化合物结构理论的主要内容是关于有机化合物分子里的原子的相互结合、排列和相互影响的学说。它的要点如下:
(1)分子里的原子按一定的顺序相互结合。
(2)分子所有原子的化合价都得到满足,没有剩余的化合价,碳原子的化合价都是四价。
(3)有机化合物的性质不但决定了它们的分子组成,而且决定于分子里原子结合的形式和顺序。
(4)分子里各原子之间是相互影响的,一般是相邻的原子或原子团影响最大。
(1)按照有机化合物中碳原子结合方式进行分类如下图:
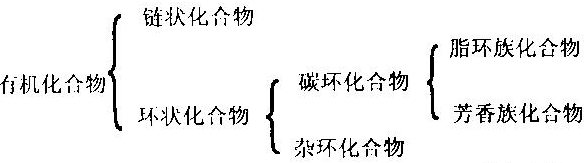
(2)按分子中组成元素的不同可分为:烃和烃的衍生物(含C、H、O、N和卤素等元素的化合物)
用元素符号表示化合物分子中元素的种类和各元素的原子数最简单整数比的式子,称为最简式或实验式。不同的有机化合物会有相同的最简式。
用一条短线连接有机化合物中各原子之间排列顺序的式子称为结构式。一条短线代表一对共用电子对。
简化了的结构式叫做结构简式。它省略了表示单键的短线,保持分子中的主要结构和官能团,能反映出各类有机化合物的主要特性,故也叫“示式性”。如乙烷和二甲醚的结构简式为:CH3-CH3;CH3-O-CH3
含有碳和氢两种元素的有机化合物统称为碳氢化合物。简称烃,例如甲烷、乙烯、乙炔、苯等。
烃分子中如果碳原子和碳原子之间都以单键相连,其余价键都是为氢原子所饱和,这类烃叫饱和烃。饱和烃中碳原子间结合的碳链如不闭合,则叫烷烃,或称链烷烃,如乙烷、丙烷,若碳链闭合成环,则叫环烷烃,如环己烷、环丙烷。
在链状烃中,碳原子之间存在双键或三键,氢原子数目比相应的烷烃少的烃称为不饱和烃。分子中有一个双键的链状烃叫烯烃。有两个双键的链状烃叫作二烯烃。有一个三键的链状烃叫炔烃。如乙烯,丁二烯,乙炔。
在烃分子中,有一个或多个由碳原子组成的环,性质与脂肪族烃相似,这类化合物成为脂环烃。
分子中有一个或多个苯环的烃称为芳香烃,简称芳烃,如苯、萘。
烃分子失去一个或几个氢原子后剩余的部分叫做烃基,常用“R-”表示,有时为书写方便,烃基可简写。如乙基CH3CH2-可写作C2H5-。常见的烃基有:甲基CH3-、乙基CH3CH2-、丙基CH3CH2CH2-、异丙基(CH3)2-CH-、苯基C6H5-。
分子中比较活泼,容易发生反应且决定化合物特性的原子或原子团,称为官能团。例如:
乙烯的(烯类)官能团结构 C=C 官能团名称:双键;
卤代烃的官能团结构X(F、Cl、Br、I)官能团名称:卤素;
醇、酚类的官能团结构-OH,名称羟基。
结构相似(有相同的官能团,化学性质相似,物力性质发生规律性变化),通式相同,在分子组成上相差一个或若干个CH2原子团的物质,互称为同系物。由同系物组成的一系列物质群,称为同系列。
例如:下列物质互为同系物
甲烷CH4、乙烷CH3CH3、丙烷CH3CH2CH3
分子式相同而结构不同的化合物,互称为同分异构体,简称异构体。
例如:分子式为C4H10的丁烷有两个同分异构体:CH3-CH2-CH2-CH3正丁烷(沸点-0.5℃),异丁烷(沸点-10.2℃)。
一种化合物分子里的某一个原子或原子团直接和间接被其他原子或原子团取代而形成的新化合物,叫作衍生物。例如卤代烃、醇、羧酸等都是烃的衍生物。
烃分子中氢被卤素原子取代后的生成物,叫作卤代烃(一卤代烃、多卤代烃),例如一氯甲烷、二氯甲烷。
链烃基与羟基相结合而构成的有机物叫做醇。可以看成醇是烃分子中的氢原子(与芳香环碳原子直接连的氢原子除外)被烃基取代后的产物(一元醇或多元醇),例如:
乙醇 CH3CH2OH 乙二醇 HO-CH2-CH2-OH
烃基与苯环直接相连而构成的化合物叫做酚。可以看成酚是苯分子中一个氢原子被羟基取代后的产物。
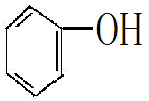
由烃基和醛基相连构成的化合物叫醛。例如:乙醛
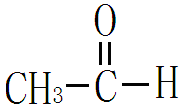
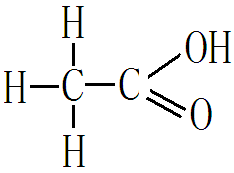
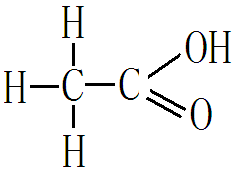
由烃基和羧酸基相连而构成的化合物叫羧酸。例如乙酸,(CH3COOH)
1.24 酯
由羧酸与醇作用脱水而成的产物叫羧酸酯。例如乙酸乙酯
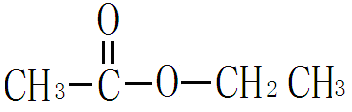
醇或酚分子中羟基上的氢原子被烃基取代后的衍生物,例如乙醚
CH3-CH2-O-CH2-CH3
1.26 硝基化合物
烃分子中的氢原子被硝基取代而生成的化合物叫硝基化合物。例如硝基苯
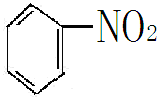
凡有机化合物中碳原子相互结合成链条状的叫作链状化合物又叫开链化合物,因为在动物的脂肪中含有这类化合物,所以也叫脂肪族化合物,例如
CH3-CH2-CH2-CH3 丁烷 CH3-COOH醋酸
1.28 环状化合物
凡有机化合物中碳原子结合成环状的叫环状化合物。又叫闭环化合物。
这类化合物中的碳原子都结合成环状,且性质和脂肪族化合物相似,例如环丙烷和环己烷。
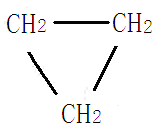
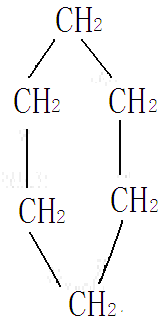 或
或 
这类化合物的碳原子环状结构中都含有苯环。

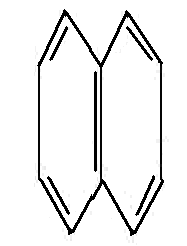
苯 萘
1.31 氧化反应
有机化合物简称有机物,是指碳氢化合物及其衍生物,有机化学是研究碳氢化合物及其衍生物的化学。
(1)熔点较低,多数有机化合物的熔点在300℃以下。
(2)容易燃烧,多数有机化合物燃烧后变成CO2和H2O。
(3)难溶于水,易溶于有机溶剂中。
(4)有机化合物不能电离,也不能导电,是非电解质。
(5)化学反应复杂,还伴有副反应发生,反应速度缓慢,且不易完成。
有机化合物除了主要元素以外,还含有少数几种其它元素,如H、O、S、P和卤素等。它们之间的结合,排列和相互影响,就在于碳的特殊性质。碳元素在形成化合物时,它既不易失去电子而形成正离子也不易获得电子而形成负离子,而是以共价键与其它原子相结合,即碳原子以四根键同其它非金属元素或金属元素结合形成分子。
例如:四氯化碳(四氯甲烷)
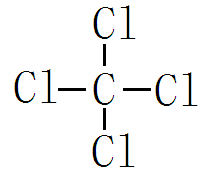
碳原子不仅能与其它原子形成共价键,碳原子与碳原子之间也能以共价键相结合,它们可以共用一个、两个或三个电子对,形成单键、双键或三键。
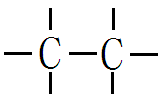

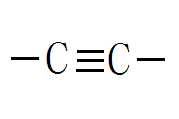
碳原子之间还可以相互结合成链状、环状、网状的有机化合物的基本骨架。
有机化合物结构理论的主要内容是关于有机化合物分子里的原子的相互结合、排列和相互影响的学说。它的要点如下:
(1)分子里的原子按一定的顺序相互结合。
(2)分子所有原子的化合价都得到满足,没有剩余的化合价,碳原子的化合价都是四价。
(3)有机化合物的性质不但决定了它们的分子组成,而且决定于分子里原子结合的形式和顺序。
(4)分子里各原子之间是相互影响的,一般是相邻的原子或原子团影响最大。
(1)按照有机化合物中碳原子结合方式进行分类如下图:
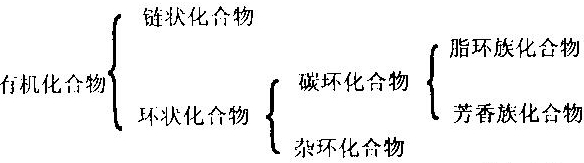
(2)按分子中组成元素的不同可分为:烃和烃的衍生物(含C、H、O、N和卤素等元素的化合物)
用元素符号表示化合物分子中元素的种类和各元素的原子数最简单整数比的式子,称为最简式或实验式。不同的有机化合物会有相同的最简式。
用一条短线连接有机化合物中各原子之间排列顺序的式子称为结构式。一条短线代表一对共用电子对。
简化了的结构式叫做结构简式。它省略了表示单键的短线,保持分子中的主要结构和官能团,能反映出各类有机化合物的主要特性,故也叫“示式性”。如乙烷和二甲醚的结构简式为:CH3-CH3;CH3-O-CH3
含有碳和氢两种元素的有机化合物统称为碳氢化合物。简称烃,例如甲烷、乙烯、乙炔、苯等。
烃分子中如果碳原子和碳原子之间都以单键相连,其余价键都是为氢原子所饱和,这类烃叫饱和烃。饱和烃中碳原子间结合的碳链如不闭合,则叫烷烃,或称链烷烃,如乙烷、丙烷,若碳链闭合成环,则叫环烷烃,如环己烷、环丙烷。
在链状烃中,碳原子之间存在双键或三键,氢原子数目比相应的烷烃少的烃称为不饱和烃。分子中有一个双键的链状烃叫烯烃。有两个双键的链状烃叫作二烯烃。有一个三键的链状烃叫炔烃。如乙烯,丁二烯,乙炔。
在烃分子中,有一个或多个由碳原子组成的环,性质与脂肪族烃相似,这类化合物成为脂环烃。
分子中有一个或多个苯环的烃称为芳香烃,简称芳烃,如苯、萘。
烃分子失去一个或几个氢原子后剩余的部分叫做烃基,常用“R-”表示,有时为书写方便,烃基可简写。如乙基CH3CH2-可写作C2H5-。常见的烃基有:甲基CH3-、乙基CH3CH2-、丙基CH3CH2CH2-、异丙基(CH3)2-CH-、苯基C6H5-。
分子中比较活泼,容易发生反应且决定化合物特性的原子或原子团,称为官能团。例如:
乙烯的(烯类)官能团结构 C=C 官能团名称:双键;
卤代烃的官能团结构X(F、Cl、Br、I)官能团名称:卤素;
醇、酚类的官能团结构-OH,名称羟基。
结构相似(有相同的官能团,化学性质相似,物力性质发生规律性变化),通式相同,在分子组成上相差一个或若干个CH2原子团的物质,互称为同系物。由同系物组成的一系列物质群,称为同系列。
例如:下列物质互为同系物
甲烷CH4、乙烷CH3CH3、丙烷CH3CH2CH3
分子式相同而结构不同的化合物,互称为同分异构体,简称异构体。
例如:分子式为C4H10的丁烷有两个同分异构体:CH3-CH2-CH2-CH3正丁烷(沸点-0.5℃),异丁烷(沸点-10.2℃)。
一种化合物分子里的某一个原子或原子团直接和间接被其他原子或原子团取代而形成的新化合物,叫作衍生物。例如卤代烃、醇、羧酸等都是烃的衍生物。
烃分子中氢被卤素原子取代后的生成物,叫作卤代烃(一卤代烃、多卤代烃),例如一氯甲烷、二氯甲烷。
链烃基与羟基相结合而构成的有机物叫做醇。可以看成醇是烃分子中的氢原子(与芳香环碳原子直接连的氢原子除外)被烃基取代后的产物(一元醇或多元醇),例如:
乙醇 CH3CH2OH 乙二醇 HO-CH2-CH2-OH
烃基与苯环直接相连而构成的化合物叫做酚。可以看成酚是苯分子中一个氢原子被羟基取代后的产物。
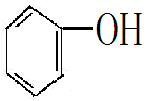
由烃基和醛基相连构成的化合物叫醛。例如:乙醛
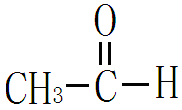
由烃基和羧酸基相连而构成的化合物叫羧酸。例如乙酸,(CH3COOH)
1.24 酯
由羧酸与醇作用脱水而成的产物叫羧酸酯。例如乙酸乙酯
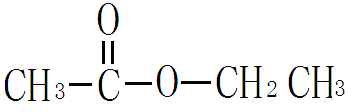
醇或酚分子中羟基上的氢原子被烃基取代后的衍生物,例如乙醚
CH3-CH2-O-CH2-CH3
1.26 硝基化合物
烃分子中的氢原子被硝基取代而生成的化合物叫硝基化合物。例如硝基苯
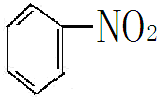
凡有机化合物中碳原子相互结合成链条状的叫作链状化合物又叫开链化合物,因为在动物的脂肪中含有这类化合物,所以也叫脂肪族化合物,例如
CH3-CH2-CH2-CH3 丁烷 CH3-COOH醋酸
1.28 环状化合物
凡有机化合物中碳原子结合成环状的叫环状化合物。又叫闭环化合物。
这类化合物中的碳原子都结合成环状,且性质和脂肪族化合物相似,例如环丙烷和环己烷。
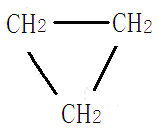
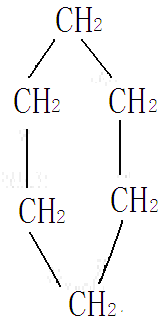 或
或 
这类化合物的碳原子环状结构中都含有苯环。
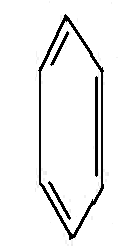
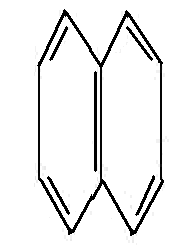
苯 萘
1.31 氧化反应
有机物可以在氧化剂的作用下发生氧化反应生成新物质。物质既可以是无机物又可以是有机物,例如:乙醇氧化成乙醛,乙醛又氧化成乙酸(醋酸);
2CH3CHO+O2=======2CH3COOH
1.32 还原反应
还原反应是含氧物质被夺去氧的单元反应。
例如:硝基苯被氢气还原为苯胺。
1.33 氢化反应
氢化反应就是有机化合物与分子氢起作用的单元反应,一般的氢化反应都有催化剂存在下进行,氢化的方法有以下几种:
(1)不饱和键加氢,如乙炔加氢转化为乙烯
H-CC-H+H2CH2=CH2
(2)环状加氢如苯环加氢转化为环己烷
C6H6+3H2C6H12
(3)含氧化合物加氢,如丁烯醛加氢制得丁醇
CH3CH=CHCH0+2H2CH3CH2CH2CH2OH
(4)含氮化合物加氢,如硝基苯加氢转化为苯胺
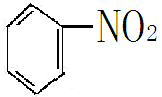 +3H2
+3H2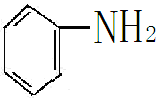 +2H2O
+2H2O
(5)氢解反应
在加氢反应过程中,同时发生分子裂解,生成分子量较小的产物。
脱氢反应是有机化合物脱去氢的单元反应。通常脱氢反应有两种:
(1)催化脱氢
使有机化合物分子中的C-H键断裂,使烷烃、烯烃和烷基芳烃转化为相应的烯烃、二烯烃和烯基芳烃。
(2)氧化脱氢
在脱氢时通入氧,使氧和氢化合成水,有利于脱氢反应进行。例如:丁烷脱氢成为丁二烯
CH3-CH2-CH2-CH3CH2=CH-CH=CH2+2H2
乙苯脱氢成苯乙烯
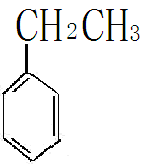
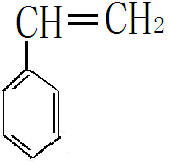 + H2
+ H2
正己烷脱氢芳香化
1.35 水合反应
水合(水化)反应就是有机化合物与水化合的反应,通常有机化合物与水分子的组分氢、氧或氢氧基(羟基)化合。
乙烯水化成乙醇
CHCH+H2O CH3CHO
乙炔水化成乙醛
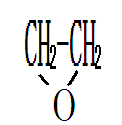 +HOHHO-CH2-CH2-OH
+HOHHO-CH2-CH2-OH
环氧乙烷水化成乙二醇
1.36 脱水反应
脱水反应是从有机化合物中脱去水的单元反应。
通常有机化合物分子中相近的两原子上的氢、氧或羟基以水分子的形式脱去。
例如:乙醇在不同条件下脱水成乙烯或乙醚
2CH3CH2OHC2H5-O-C2H5+H2O
1.37 水解反应
水解反应是物质与水作用所引起双分解的单元反应。
水解反应可分为三种类型:
(1)无机盐在水中的分解
一般强酸和弱碱生成的盐(如NH4Cl)强碱和弱酸生成的盐(如Na2CO3)和弱酸弱碱所生成的盐如(CH3COONH4)遇水都发生分解反应。
NH4CL+H2ONH4OH+HCL
Na2CO3+H2ONaOH+NaHCO3
CH3COONH4+H2O NH4OH+CH3COOH
(2)有机化合物在酸性溶液中水解
醋酸乙酯水解为醋酸和乙醇:
CH3COOC2H5+H2O======CH3COOH+C2H5OH
蔗糖水解为葡萄糖和果糖
C12H22O11+H2OC6H12O6+C6H12O6
葡萄糖 果糖
(3)有机化合在碱性溶液中的水解
油脂在碱作用下水解生成甘油和钠肥皂。酯在碱性溶液中的水解反应又叫皂化反应。
(C17H35COO)3C3H5+3NaOH=====C3H5(OH)3+3C17H35COONa
有机物可以在氧化剂的作用下发生氧化反应生成新物质。物质既可以是无机物又可以是有机物,例如:乙醇氧化成乙醛,乙醛又氧化成乙酸(醋酸);
2CH3CHO+O2=======2CH3COOH
1.32 还原反应
还原反应是含氧物质被夺去氧的单元反应。
例如:硝基苯被氢气还原为苯胺。
1.33 氢化反应
氢化反应就是有机化合物与分子氢起作用的单元反应,一般的氢化反应都有催化剂存在下进行,氢化的方法有以下几种:
(1)不饱和键加氢,如乙炔加氢转化为乙烯
H-CC-H+H2CH2=CH2
(2)环状加氢如苯环加氢转化为环己烷
C6H6+3H2C6H12
(3)含氧化合物加氢,如丁烯醛加氢制得丁醇
CH3CH=CHCH0+2H2CH3CH2CH2CH2OH
(4)含氮化合物加氢,如硝基苯加氢转化为苯胺
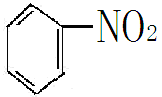 +3H2
+3H2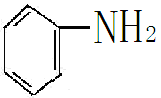 +2H2O
+2H2O
(5)氢解反应
在加氢反应过程中,同时发生分子裂解,生成分子量较小的产物。
脱氢反应是有机化合物脱去氢的单元反应。通常脱氢反应有两种:
(1)催化脱氢
使有机化合物分子中的C-H键断裂,使烷烃、烯烃和烷基芳烃转化为相应的烯烃、二烯烃和烯基芳烃。
(2)氧化脱氢
在脱氢时通入氧,使氧和氢化合成水,有利于脱氢反应进行。例如:丁烷脱氢成为丁二烯
CH3-CH2-CH2-CH3CH2=CH-CH=CH2+2H2
乙苯脱氢成苯乙烯
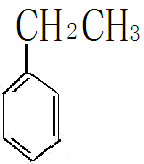
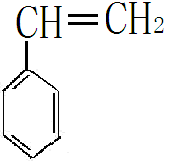 + H2
+ H2
正己烷脱氢芳香化
1.35 水合反应
水合(水化)反应就是有机化合物与水化合的反应,通常有机化合物与水分子的组分氢、氧或氢氧基(羟基)化合。
乙烯水化成乙醇
CHCH+H2O CH3CHO
乙炔水化成乙醛
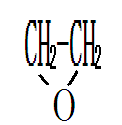 +HOHHO-CH2-CH2-OH
+HOHHO-CH2-CH2-OH
环氧乙烷水化成乙二醇
1.36 脱水反应
脱水反应是从有机化合物中脱去水的单元反应。
通常有机化合物分子中相近的两原子上的氢、氧或羟基以水分子的形式脱去。
例如:乙醇在不同条件下脱水成乙烯或乙醚
2CH3CH2OHC2H5-O-C2H5+H2O
1.37 水解反应
水解反应是物质与水作用所引起双分解的单元反应。
水解反应可分为三种类型:
(1)无机盐在水中的分解
一般强酸和弱碱生成的盐(如NH4Cl)强碱和弱酸生成的盐(如Na2CO3)和弱酸弱碱所生成的盐如(CH3COONH4)遇水都发生分解反应。
NH4CL+H2ONH4OH+HCL
Na2CO3+H2ONaOH+NaHCO3
CH3COONH4+H2O NH4OH+CH3COOH
(2)有机化合物在酸性溶液中水解
醋酸乙酯水解为醋酸和乙醇:
CH3COOC2H5+H2O======CH3COOH+C2H5OH
蔗糖水解为葡萄糖和果糖
C12H22O11+H2OC6H12O6+C6H12O6
葡萄糖 果糖
(3)有机化合在碱性溶液中的水解
油脂在碱作用下水解生成甘油和钠肥皂。酯在碱性溶液中的水解反应又叫皂化反应。
(C17H35COO)3C3H5+3NaOH=====C3H5(OH)3+3C17H35COONa

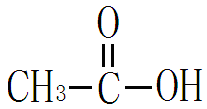
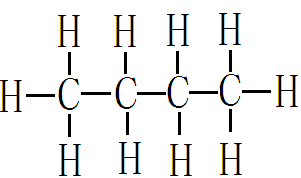
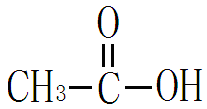
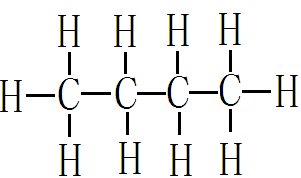
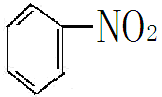 +3H3
+3H3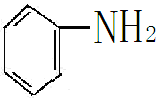 +2H2O
+2H2O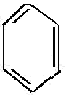 +4H2O
+4H2O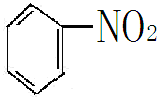 +3H3
+3H3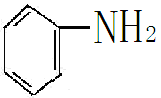 +2H2O
+2H2O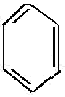 +4H2O
+4H2O